Juan Armando Sánchez*, Julio Andrade*, Luisa F. Dueñas**, Carlos Edwin Gómez*
Todos los interesados en el estudio del cambio climático y sus efectos en la biodiversidad buscamos la manera de predecir las consecuencias biológicas de las elevadas temperaturas, así como la variación en las comunidades afectadas. Sin embargo, muy pronto, al empezar nuestras investigaciones, nos damos cuenta de la complejidad de este problema. Particularmente, los que trabajamos en el mar envidiamos a nuestros pares continentales que predicen con mapas el movimiento altitudinal y latitudinal de los ecosistemas.
En el mar el cambio climático no es un escenario del futuro, pero anticipar su impacto y magnitud es aún muy difícil. Desde inicios de la década de 1980, y posiblemente antes, se han presentado anomalías térmicas relacionadas con el aumento de las temperaturas, las cuales han estado asociadas a eventos extremos que se han detectado en todos los océanos a manera de “olas de calor” (MHW por su sigla en inglés) afectando diferentes ecosistemas marinos, entre ellos los arrecifes de coral [1,2]. Sin embargo, estas manifestaciones son difíciles de predecir, así como los efectos que tendrán las anomalías térmicas sobre los ecosistemas marinos.
En este artículo presentamos inicialmente un breve recuento de la evidencia del cambio climático y sus efectos en organismos arrecifales. Más adelante, presentaremos un recuento de la investigación en el Pacífico Oriental Tropical (POT) colombiano (figura 1), por parte del grupo de Biología Molecular Marina (Biommar) de la Universidad de los Andes, , para finalmente presentar datos de las observaciones de la temperatura del mar entre 2003-2011 en esta misma región.
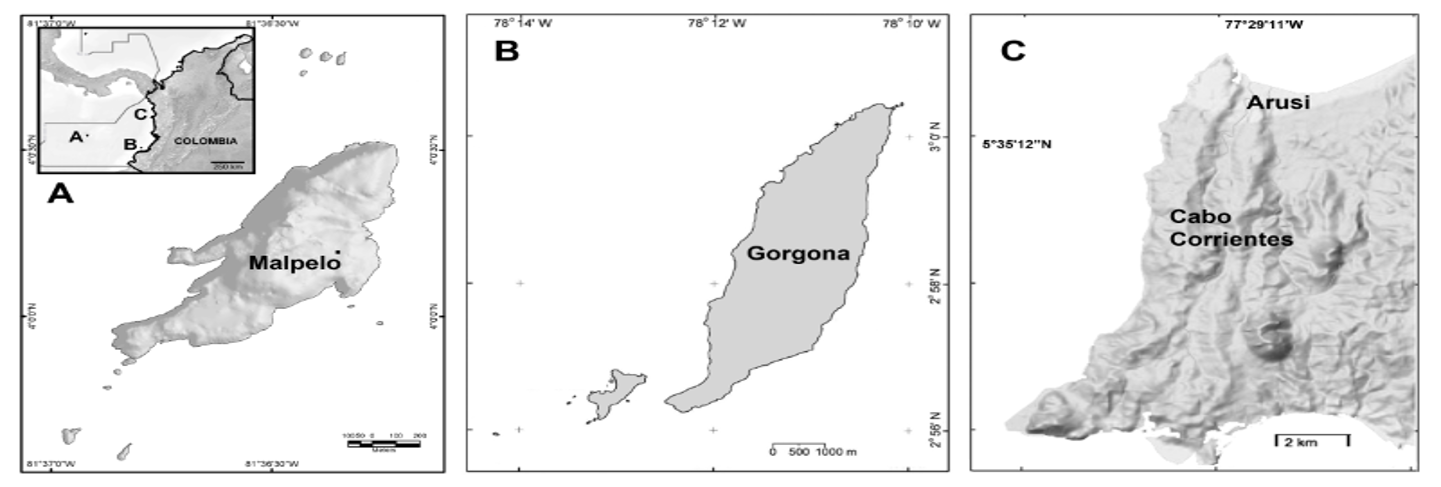
Figura 1. Localidades donde se ha enfocado la investigación en los efectos de las elevadas temperaturas del agua y el cambio global en el Pacífico Oriental Tropical (POT) de Colombia. A. Isla Malpelo, B. Isla Gorgona, C. Cabo Corrientes, Choco [3].
Respuestas a las anomalías térmicas en organismos arrecifales
A finales de 1982 y principios de 1983 se presentaron las mayores mortalidades de corales jamás registradas en los mares tropicales de América. El fenómeno de El Niño Oscilación Sur (ENSO por su sigla en inglés) del 82-83, con una anomalía térmica que se prolongó por 10 meses, causó mortandades coralinas cercanas al 70-90 % en Colombia, Panamá y Costa Rica, y mayores al 95 % en las islas Galápagos [4]. Simultáneamente, en los arrecifes coralinos del Atlántico occidental, a causa de una enfermedad microbiana, desaparecían los corales cuerno de ciervo y cuerno de alce, Acropora palmata y A. cervicornis, principales constructores arrecifales [5]. Por causas similares, entre enero de 1983 y enero de 1984 desaparece el 99 % de los individuos del erizo negro, Diadema antillarum, en todo el Atlántico tropical [6]. En esta misma época se registra otra mortalidad masiva en los abanicos de mar del género Gorgonia [7,8], afectando uno de los elementos paisajísticos clave del Caribe. Desde entonces, los arrecifes coralinos del POT y del Atlántico occidental no han regresado a su estado original y empeoran con cada evento perturbador.
La situación de los ecosistemas marinos en América tropical, y en especial de los arrecifes coralinos, ha venido empeorando por la sinergia con otros factores como las tormentas tropicales, la explotación de sus recursos y la eutrofización producto del desarrollo continental y costero. El Atlántico occidental ha venido en constante decline desde entonces, superando los umbrales del punto de no retorno, en que los arrecifes han pasado de ser dominados por corales a algas [9].
Otras regiones del mundo, como la Gran Barrera de Coral y los arrecifes del Indopacífico, han venido sufriendo mortalidades coralinas producto de blanqueamiento coralino, o expulsión de las microalgas dinoflageladas simbióticas conocidas como zooxantelas (Symbiodiniaceae: Zoophyta), registrándose un gran evento mundial de blanqueamiento durante 1998 [10]. Posteriormente, el blanqueamiento coralino ha sido un factor de deterioro coralino recurrente en los arrecifes coralinos de todo el mundo.
Gracias al sistema de alerta temprana de blanqueamiento coralino de NOAA ‘Coral Reef Watch’ (National Oceanographic and Atmospheric Administration, E.E.U.U.) se ha podido alertar en tiempo real a la comunidad científica sobre eventos de blanqueamiento. En el 2005, por ejemplo, una anomalía térmica (temperaturas por encima del máximo histórico de los últimos 150 años) que se prolongo por 16 semanas ocasionó un blanqueamiento del 80% de los corales del Atlántico occidental tropical, incluyendo el Caribe colombiano, con mortalidades de hasta el 40% [11]. El 2005 es también el año con el record de huracanes en el Atlántico, cuatro de ellos de categoría 5, incluyendo el huracán Katrina.
¿Estará esto relacionado con el cambio climático?
Un fenómeno similar se presentó durante el 2010, esta vez afectando también grandes extensiones coralinas del Indopacífico [12]. El 2010 es el tercer año en la historia en términos de huracanes y tormentas tropicales. Los récords fueron superados por el 2021 con 30 huracanes que, aunque de menor magnitud, son una alarma para los próximos años. Paralelamente, mortandades coralinas debidas a enfermedades microbianas, pero de distribución más localizada, también han sido relacionadas con elevadas temperaturas del agua [13]. En definitiva, las últimas tres décadas nos muestran dos aspectos claros: (1) las anomalías térmicas, relacionadas o no con ENSO, son cada vez más frecuentes, y (2) las peores mortalidades coralinas en todo el mundo están directamente relacionadas con estas anomalías térmicas.
Situación de los octocorales en el POT
Desde finales de la última década se han observado por primera vez dos situaciones anormales en los octocorales del POT. Los octocorales de aguas someras de esta región conforman una diversa y endémica fauna de gorgonáceos tipo candelabro, látigo y abanico, pertenecientes principalmente a las familias Gorgoniidae y Plexauridae [14]. A diferencia de la fauna de octocorales del mar Caribe, en esta región todas las especies carecen de zooxantelas y son filtradores suspensívoros activos que se encuentran en los infralitorales sobre fondos duros. Sus colonias de hasta 1 m de altura pueden dominar el paisaje de estos litorales con densidades de hasta 30 colonias por metro cuadrado [3,15]. Géneros como Pacifigorgia pueden tener hasta 35 especies en esta región donde cada vez se descubren especies nuevas [16] y cada especie de coral potencialmente alberga otras especies de organismos asociados que son únicos y/o nuevos para la ciencia [15,17].
Pese a las características únicas de la fauna de octocorales del POT, así como su gran importancia ecológica, es una de las áreas del mundo con menos estudios ecológicos. Situación lamentable dado que en la última década se han documentado varias enfermedades y especies invasoras que ponen en riesgo la comunidad de octocorales.
Durante el 2008 ocurrió una mortandad masiva de los abanicos de mar del género Pacifigorgia en la isla Gorgona, donde un 70 % de las colonias de cuatro especies murieron [3,18]. Esto coincide con estudios microbiológicos de las mismas especies presentando síntomas de enfermedades fúngicas desde el 2007 [19]. De manera similar, en la región de Cabo Corrientes e isla Malpelo fueron observadas mortandades de abanicos de mar [15,18]. Estos episodios muestran un panorama muy parecido a lo que ocurrió durante principios de los años ochenta en el mar Caribe con la desaparición de los abanicos de mar del género Gorgonia. En ese entonces se le atribuyó el fenómeno a una enfermedad fúngica caracterizada por la infección del hongo Aspergillus sydowi, cuya epizootiología se presenta en relación con elevadas temperaturas del agua (Alker et al., 2001). La prevalencia de la enfermedad continúa desde entonces en el POT colombiano (figura 2A) y en localidades como isla Gorgona las poblaciones de abanicos de mar están amenazadas con extinción local.
No fue hasta que gracias a métodos de metabarcoding logramos estudiar la microbiota de Pacifigorgia. Esta comunidad la conforman más de 300 tipos de bacterias y otros microorganismos, muchas de estas endosimbióticas.

Figura 2A. Octocorales del género Pacifigorgia. Colonia de Pacifigorgia irene con muestras de una lesión fúngica en Cabo Corrientes, Chocó, Colombia.
La microbiota de las colonias de Pacifigorgia enfermas no se diferenciaban en la composición con respecto a las colonias sanas, pero se notaba un cambio en la abundancia de microorganismos en donde aumentaban aleatoriamente algunos tipos raros, quizás oportunistas, mientras los principales, importantes para la nutrición, disminuían abruptamente [20]. No se encontró un agente patógeno como tal sino una ruptura del equilibro de la microbiota, una disbiosis, que conducía a la enfermedad y posteriormente daba paso a los hongos que deshacían el tejido coralino. En este caso, no se trataba de una enfermedad infecciosa sino de un desequilibrio en la microbiota.
Otro factor de gran preocupación para la conservación de los octocorales del POT, y otras especies del litoral, es la presencia del coral copo de nieve (Carijoa riisei: figura 2B). Considerada originaria del Indopacífico [21], C. riisei, se halló fuera de su rango natural en los años setenta en el archipiélago de Hawái, donde arrasó con las poblaciones de coral negro provocando el cierre de su pesquería para la joyería del coral [22].
Este coral blando invasor se encuentra en simbiosis con una esponja, Desmapsamma anchorata, cuyas sustancias citotóxicas le confieren una gran superioridad competitiva frente a otros organismos arrecifales, provocando necrosis del tejido blando de otros octocorales y apoderándose rápidamente de sus esqueletos [23]. Aunque esta especie lleva más de 15 años en el POT [24], hasta hace poco se ha documentado el comportamiento agresivo y el ahogamiento que produce esta especie sobre los octocorales nativos de esta región [25]. La especie invasora en unos pocos meses se logra posesionar de grandes áreas de litorales entre 5 y 20 m, arrasando con casi todas las especies de octocorales y otros invertebrados sésiles. Se presume que el contacto con C. riisei puede aumentar la frecuencia de enfermedades fúngicas y que los candelabros del género Muricea están localmente extintos, en muchas regiones del POT, en relación con la presencia de esta especie invasora.
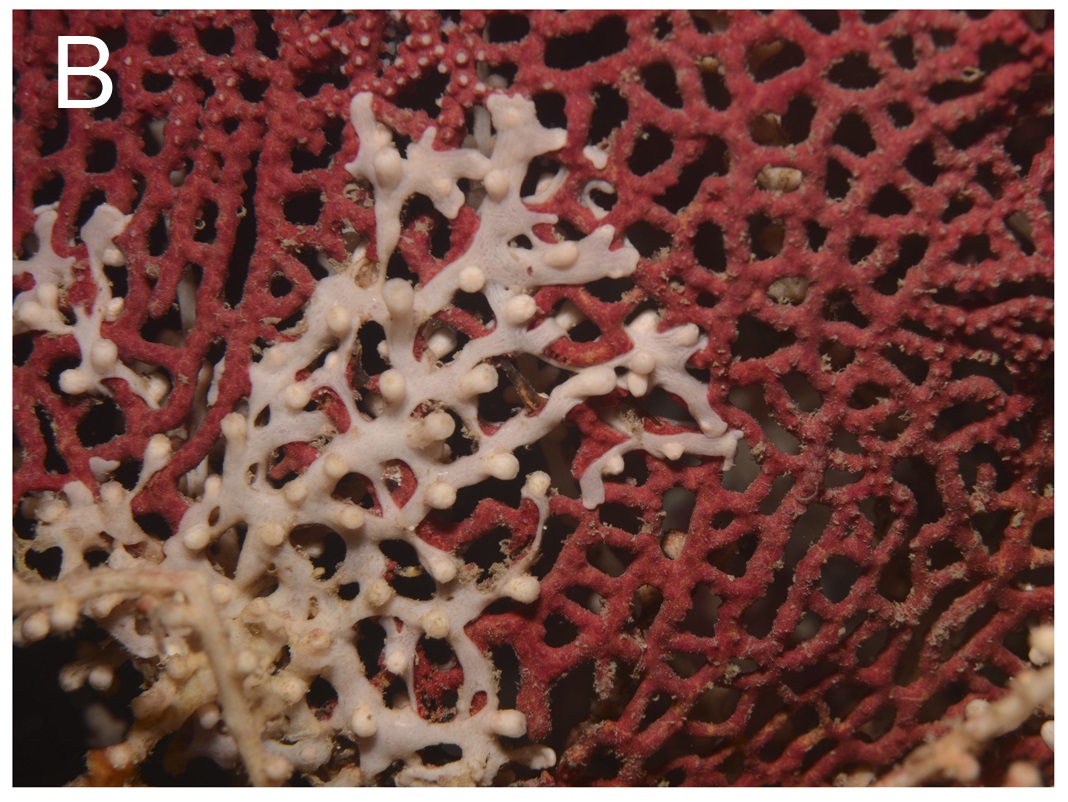
Figura 2B. Octocorales del género Pacifigorgia. Detalle de una colonia de P. rubicunda presentando cubrimiento por la especie invasora Carijoa riisei en isla Gorgona, Colombia.
Otra potencial amenaza: acidificación oceánica
La acidificación oceánica, también conocida como el otro problema del cambio climático, es la disminución del pH del agua del mar a causa del incremento del CO2 atmosférico producto de la industrialización y quema de combustibles fósiles [26]. Debido a que los océanos cumplen una función muy importante en la regulación del CO2 atmosférico al incorporar de forma natural este gas, se ha estimado que alrededor del 50 % del CO2 generado antropogénicamente desde el siglo XX, ha sido incorporado por los océanos [27,28], incrementando así la presión parcial desde 280 partes por mil (ppm) en la era preindustrial (siglo XIX), a casi 420 ppm para febrero del 2022, lo que ha conllevado a una disminución del pH de aproximadamente 0,06 unidades en los últimos 30 años [29]. Se tiene evidencia de que esta concentración de CO2 atmosférico posiblemente ha sido la más alta reportada en los últimos 650.000 años [30].
La disminución en el pH tiene como principal consecuencia la disminución de los estados de saturación del carbonato de calcio (CaCO3) que es importante para diferentes organismos marinos que dependen de él para formar sus esqueletos y/o conchas. Particularmente, los arrecifes de coral se encuentran entre los ecosistemas marinos más vulnerables por la acidificación oceánica por ser uno de los que más depende de la saturación del CaCO3, lo que pone en riesgo su estabilidad y perdurabilidad a largo plazo [31].
Los octocorales no son considerados importantes constructores de arrecifes coralinos, sin embargo, diferentes estudios han señalado la importancia de este grupo como formadores de sedimentos y formadores de estructuras calcáreas significativas, como lo es la espiculita, que es una formación rocosa mineral compuesta principalmente por escleritos de octocorales que puede estar contribuyendo al crecimiento arrecifal [32,33]. Sumado a esto, aproximadamente el 80 % del peso seco de algunos octocorales está compuesto por escleritos de carbonato de calcio que aportan hasta un 2 % del total de carbonato en arrecifes del Caribe [34]. En el POT colombiano el grupo de los octocorales es dominante en los arrecifes rocosos en la franja costera continental somera y en zonas oceánicas como la isla Malpelo, donde existe una dominancia de esta comunidad formando en su mayoría agrupaciones de altas densidades, sobre todo en zonas someras de los escarpes rocosos [18].
No obstante, existe evidencia natural de que los efectos de una posible acidificación oceánica global podrían traer repercusiones negativas para los ecosistemas de arrecifes coralinos en el POT, debido a que las aguas del océano Pacífico alcanzan estados insaturados a profundidades menores que las encontradas en el océano Atlántico [35].

Figura 3. Registro fotográfico de colonias de Pacifigorgia cairnsii tomadas en diciembre de 2012 y marzo de 2013 en isla Malpelo. A – B. Colonia con crecimiento positivo y recuperación de tejido entre diciembre de 2012 y marzo de 2013 sin presencia de enfermedad. C – D. Colonia completamente regenerada y sin presencia de enfermedad y E – F. Colonia con presencia de enfermedad en diciembre de 2012, y completamente sana y regenerada en marzo de 2013. (Las flechas rojas indican sitios con presencia de tejido muerto y luego de sanar).
Estas aguas profundas tienen concentraciones de CO2 más altas y pH más bajos producto de la oxidación de material vegetal orgánico. Debido a que el POT está directamente influenciado por procesos de surgencia que traen a la superficie estas aguas profundas ricas en CO2, procesos de acidificación oceánica se podrían ver más acentuados limitando así el desarrollo coralino. Manzello y colaboradores estudiaron tres arrecifes de esta zona y los compararon con datos de un arrecife de Bahamas con características opuestas [36]. Los resultados encontrados mostraron que la poca cementación existente y, por consiguiente, el bajo desarrollo de corales duros en esta zona está influenciado por estas condiciones oceanográficas características, donde se presenta una acidificación oceánica local que es causa de tasas de bioerosión que superan las de acreción. De este estudio se puede concluir que futuros escenarios de acidificación oceánica podrían estar limitando un desarrollo arrecifal complejo.
Efectivamente, entre los sitios estratégicos que se han seleccionado o propuesto para implementar con urgencia estudios de monitoreo se encuentra toda la zona que comprende el POT, donde islas como Malpelo se encuentran dentro de un sector sensible a la acidificación oceánica [26].
La importancia de los corales para sobrevivir y recuperarse de algún disturbio es crítica para la permanencia y subsistencia de las poblaciones [37]. La regeneración de tejido vivo en octocorales está gobernada por ciertas características morfológicas análogas a las encontradas en plantas, lo que les favorece un rápido crecimiento y capacidad regenerativa [38].
Además, la regeneración de tejido está íntimamente relacionada con la precipitación de carbonato de calcio (CaCO3) a manera de escleritos por medio de un proceso biológico llamado calcificación. Sin duda, es una parte integral de la supervivencia y es esencial para la comunidad porque permite la recuperación debido a diferentes disturbios tanto naturales como antrópicos. En la isla Malpelo se ha estado monitoreando la comunidad de octocorales ubicada en los escarpes rocosos en diferentes sitios de la isla. Estudios de crecimiento, regeneración y estado de salud, sugieren una comunidad de octocorales de las especies Pacifigorgia cairnsi, P. curta y Leptogorgia alba bastante resiliente.
Se ha encontrado que las diferentes poblaciones han sufrido periodos de enfermedad y pérdida de tejido coralino vivo cercanos al 50 %, no obstante, se ha observado recuperación de un periodo a otro en relación con los ciclos de ENSO [39]. Como ejemplo, en diciembre del 2012 la incidencia de colonias enfermas y con pérdida de tejido estuvo cercana al 50 % para algunos sectores de la isla, recuperándose por completo para el mes de marzo del 2013 cuando se visitaron nuevamente dichas poblaciones. Así mismo, la toma de datos de regeneración del tejido de Pacifigorgia cairnsii se ha venido realizando mediante seguimiento fotográfico.
Resultados preliminares también concuerdan con los datos de estado de salud, encontrándose que más del 70 % de las colonias que se habían fotografiado en diciembre del 2012 se encontraban completamente regeneradas y sanas (figura 3). También, se ha podido observar pérdida de tejido en algunas de las colonias que se encontraban con algún grado de enfermedad, sin embargo, esto no ha comprometido la sobrevivencia de las colonias hasta este momento.
Recientes estudios llevados a cabo en ambientes naturales de alto CO2 han dado evidencia del posible poder adaptativo y de resiliencia de los octocorales hacia efectos de acidificación oceánica [40], lo que se ha demostrado igualmente en condiciones controladas [41]. En estos ambientes las condiciones naturales reflejan altas concentraciones de CO2 y estados de baja saturación de carbonatos como los que se podrían experimentar en algunas zonas del POT [42]. Estos resultados han dado una clara evidencia de cómo la acidificación oceánica proyectada a ocurrir en los próximos 200-300 años (dependiendo del escenario que se elija), podría conllevar un cambio de fase de organismos duros a organismos blandos y autótrofos (con asociaciones simbióticas algales). No obstante, la información aún es muy limitada y se requieren de estudios que investiguen la sinergia de la acidificación oceánica con los cambios de temperatura proyectados para ocurrir a final del siglo XXI, para así poder tener un mejor panorama del poder de resiliencia de los octocorales en el Pacífico Oriental Tropical.
Tendencias en la temperatura del agua en el POT
Desde el inicio del milenio, las tendencias de la temperatura marina superficial para el POT presentan anomalías térmicas sostenidas (figura 4). Con el fin de evaluar en detalle las tendencias en los cambios de temperatura para el POT colombiano, utilizamos los datos de nuestros estudios anteriores y se exploraron las temperaturas desde el 2003 al 2011. Debido a que la temperatura de cada lugar puede estar relacionada con su ubicación geográfica (cercanía a la costa), y con los patrones de corrientes tanto unidireccionales como verticales (eventos de surgencia), no es prudente dar una tendencia general para el cambio de temperatura en el POT colombiano. Por esta razón, se mirará en detallada para la isla Malpelo.
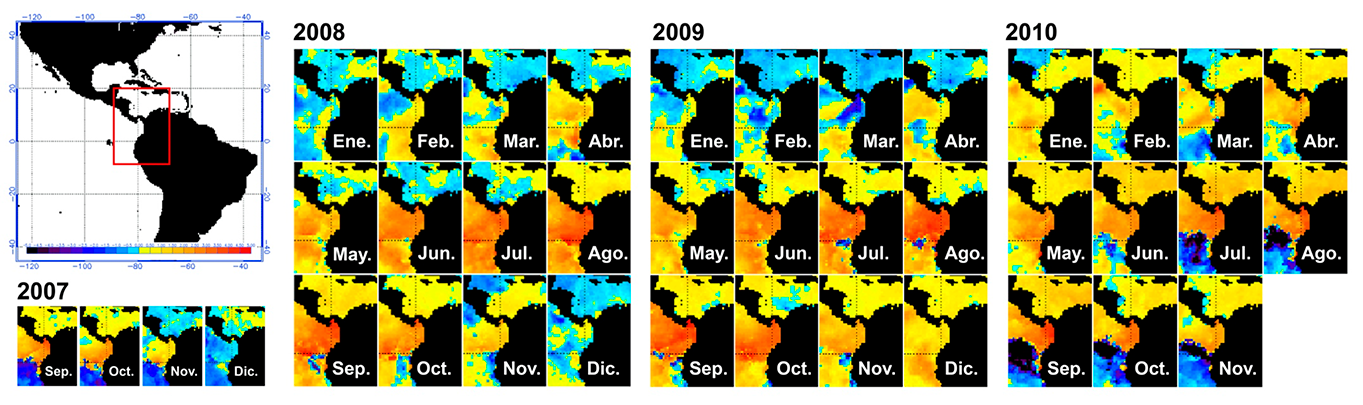
Figura 4. Anomalías térmicas para el Pacífico Oriental Tropical durante los años 2007, 2008, 2009 y 2010. Los mapas a color muestran las anomalías térmicas para cada mes. Una anomalía positiva significa que la actual temperatura superficial del mar es mas cálida que el promedio (tonalidades naranja-rojizas) y una anomalía negativa significa que es mas fría que el promedio (tonalidades azules-moradas). Fuentes NOAA http://www.osdpd.noaa.gov/ml/ocean/sst/anomaly.html y NOAA Coral Reef Watch, http://coralreefwatch.noaa.gov/satellite/.
Temperatura en el agua de la Isla Malpelo
Malpelo es una isla oceánica ubicada a 500 km de la costa colombiana. Es una formación rocosa que data del Mioceno y es la única porción de la Dorsal de Malpelo que emerge del agua. Sus características oceanográficas únicas hacen de Malpelo un lugar altamente biodiverso en organismos marinos, y en 1995 fue declarada Santuario de Flora y Fauna, y en el 2006 Patrimonio de la Humanidad.
La temperatura diaria promedio muestra una estacionalidad marcada. En los meses de enero a abril se observa una reducción en la temperatura y una alta variación en la misma (figura 5 inferior), patrón que se ve claramente al estimar el cambio en el promedio diario móvil (figura 5 superior). Durante los meses de junio a diciembre se ve una reducción en la variación (valores cercanos a cero; figura 5 superior) y una estabilidad en la temperatura entre los 24 y 26 °C.
Las temperaturas más altas registradas fueron de 31,92 °C para mayo del 2009 y de 31,64 °C para agosto del 2011. La temperatura más baja corresponde a 16,75 °C para abril del 2006.
Al comparar el mismo mes durante la serie temporal es posible observar de manera más clara el comportamiento de la temperatura a lo largo del tiempo. Enero muestra una tendencia de reducción de temperatura, siendo 0,398 °C más frío cada año (figura 5). Por el contrario, los meses de febrero, marzo, abril, mayo, junio y agosto muestran un incremento de temperatura al año por encima de 0,1 °C. Los meses de julio y octubre también tienen una tendencia de incremento de temperatura, pero es más moderada, estando por debajo de 0,1 °C al año.
Finalmente, los meses de septiembre, noviembre y diciembre no revelan ninguna tendencia significativa, mostrándose estables desde el 2003 al 2011 (figura 5).
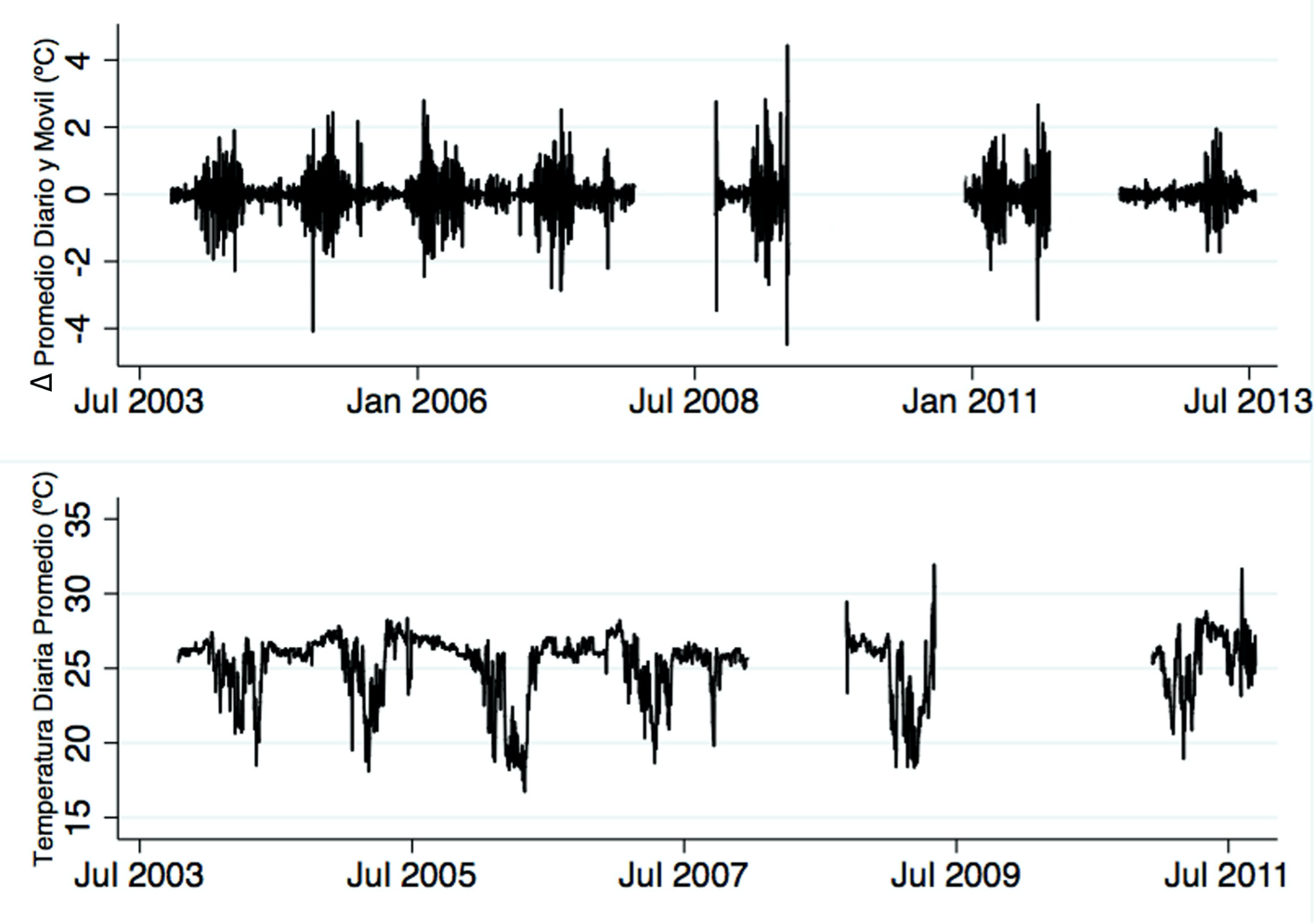
Figura 5. Evolución de la temperatura del año 2003 al 2013. Arriba se representa la diferencia del promedio diario de temperatura (ºC) y el promedio móvil (se promedio t-1, t y t+1) para toda la secuencia. Abajo se representa el promedio diario de la temperatura (ºC).
Teniendo en cuenta la variación de la temperatura a lo largo del año en Malpelo, donde las tendencias sugieren variaciones sostenidas año tras año, se puede afirmar que las dinámicas naturales de los ecosistemas marinos se verán afectados en el mediano plazo. Como se observa en la figura 6, los parámetros de la regresión realizada en las series de tiempo de cada mes, confirman que ocho meses del año se están volviendo más calientes (p < 0,05), con máximos de aumento cercanos a 0,6 °C por año, tendencia que de mantenerse en el futuro tendrá resultados catastróficos para los ecosistemas marinos costeros de la región de Malpelo.
Para finalizar, podemos decir que existe evidencia que la comunidad de octocorales del POT está siendo afectada puntual o prolongadamente por anomalías térmicas, las cuales parecen estar relacionadas con el cambio climático. Específicamente las poblaciones que se encuentran en la parte oceánica como la isla Malpelo, presentan un grado de resiliencia hacia procesos naturales como respuesta a enfermedades y posterior recuperación. No obstante, la evidencia hacia procesos de cambio climático y acidificación del océano son aún muy incipientes, y generan la necesidad de realizar estudios más específicos. Recomendamos de manera prioritaria acciones de monitoreo y red de medición de las temperaturas y la termoclina en el POT. Asimismo, implementar un estudio de caracterización y monitoreo de la química del agua (carbonatos, bicarbonatos, estados de saturación de aragonita y calcita) en los diferentes sitios donde se ha realizado el seguimiento de las poblaciones de octocorales del POT.
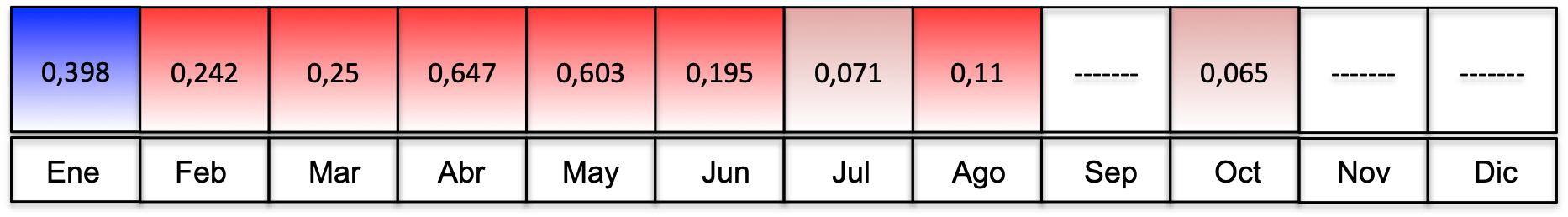
Figura 6. Resultados de la regresión por MCO de temperatura y tiempo. Los parámetros de cada regresión se muestran en la figura para los meses que fueron relevantes (p<0,05). El color azul indica que la tendencia es negativa, o de enfriamiento, el rojo fuerte indica aumento mayor a 0,1ºC por año y el rojo claro indica aumentos significativos menores a 0,1ºC por año.
Referencias
[1] Frölicher TL, Laufkötter C. Emerging risks from marine heat waves. Nature communications. 2018;9: 650.
[2] Oliver ECJ, Burrows MT, Donat MG, Sen Gupta A, Alexander LV, Perkins-Kirkpatrick SE, et al. Projected Marine Heatwaves in the 21st Century and the Potential for Ecological Impact. Frontiers in Marine Science. 2019;6: 734.
[3] Sánchez JA, Ardila NE, Andrade J, Dueñas LF, Navas R, Ballesteros D. Octocoral densities and mortalities in Gorgona Island, Colombia, Tropical Eastern Pacific. Revista de Biología Tropical. 2014;62: 209–219.
[4] Fong P, Glynn PW. A regional model to predict coral population dynamics in response to El Niño southern oscillation. Ecological Applications. 2000;10: 842–854.
[5] Glynn PW, Peters EC, Muscatine L. Coral tissue microstructure and necrosis: relation to catastrophic coral mortality in Panama. DisAquat Org. 1985;1: 29–37.
[6] Lessios HA, Robertson DR, Cubit JD. Spread of Diadema mass mortality through the Caribbean. Science. 1984;226: 335– 337.
[7] Guzmán HM, Cortés J. Mortandad de Gorgonia flabellum Linnaeus. Revista de Biologia Tropical. 1984;32: 304–308.
[8] Garzón-Ferreira J, Zea S. Mass mortality of Gorgonian ventalina (Cnidaria: Gorgoniidae in the Santa Marta area, Caribbean coast of Colombia. Bulletin of Marine Science. 1992;50: 522–526.
[9] Gardner TA, Cote IM, Gill JA, Grant A, Watkinson AR. Long-term region-wide declines in Caribbean corals. Science. 2003;301: 958–961.
[10] Hoegh-Guldberg O, Mumby PJ, Hooten AJ, Steneck RS, Greenfield P, Gomez E, et al. Coral reefs under rapid climate change and ocean acidification. Science. 2007;318: 1737–1742.
[11] Eakin CM, Morgan JA, Heron SF, Smith TB, Liu G, AlvarezFilip L, et al. Caribbean corals in crisis: record thermal stress, bleaching, and mortality in 2005. PloS One. 2010;5: e13969.
[12] Guest JR, Baird AH, Maynard JA, Muttaqin E, Edwards AJ, Campbell SJ, et al. Contrasting patterns of coral bleaching susceptibility in 2010 suggest an adaptive response to thermal stress. PLoS One. 2012;7: e33353.
[13] Sánchez JA, S. Herrera, R. Navas-Camacho, A. Rodríguez-Ramírez, P. Herron, V. Pizarro, et al. White plague-like coral disease in remote reefs of the Western Caribbean. Revista de Biología Tropical. 2010;58: 145–154.
[14] Sánchez JA, Dueñas, L.F., Rowley, S.J., González , F.L., Vergara, D.C., Montaño-Salazar , S.M., et al. Gorgonian Corals. Loya Y, Puglise K, Bridge T Mesophotic Coral Ecosystems. Springer Nature Switzerland AG; 2019. 727–745.
[15] Sánchez JA. Diversity and evolution of octocoral animal forests at both sides of tropical America. Marine Animal Forests: The Ecology of Benthic Biodiversity Hotspots. 2017. 111–143.
[16] Vargas S, Guzman HM, Breedy O. Distribution patterns of the genus Pacifigorgia (Octocorallia: Gorgoniidae): track compatibility analysis and parsimony analysis of endemicity. J Biogeogr. 2008;35: 241–247.
[17] Sánchez JA, Fuentes-Pardo AP, Almhain ÍN, Ardila-Espitia NE, Cantera-Kintz J, Forero-Shelton M. The Masquerade Game: marine mimicry adaptation between egg-cowries and octocorals. PeerJ. 2016;4:e2051.
[18] Sánchez JA, Gómez CE, Escobar D, Dueñas LF. Diversidad, abundancia y amenazas de los octocorales de la isla Malpelo, Pacífico Oriental Tropical, Colombia.Boletín de Investigaciones Marinas y Costeras-INVEMAR. 2011;40: 139–154.
[19] Barrero-Canosa J, Dueñas LF, Sánchez JA. Isolation of potential fungal pathogens in gorgonian corals at the Tropical Eastern Pacific. Coral Reefs. 2013;32: 35–41.
[20] Quintanilla E, Ramírez-Portilla C, Adu-Oppong B, Walljasper G, Glaeser SP, Wilke T, et al. Local confinement of disease-related microbiome facilitates recovery of gorgonian sea fans from necrotic-patch disease. Scientific reports. 2018;8: 14636.
[21] Concepcion G, Kahng S, Crepeau M, Franklin E, Coles S, Toonen R. Resolving natural ranges and marine invasions in a globally distributed octocoral (genus Carijoa). Marine Ecology Progress Series. 2010;401: 113–127.
[22] Kahng SE, Grigg RW. Impact of an alien octocoral, Carijoa riisei, on black corals in Hawaii. Coral Reefs. 2005;24: 556–562.
[23] Calcinai B, Bavestrello G, Cerrano C. Dispersal and association of two alien species in the Indonesian coral reefs: the octocoral Carijoa riisei and the demosponge Desmapsamma anchorata. Journal of the marine Biological Association of the United Kingdom. 2004;84: 937–941.
[24] Quintanilla E, Wilke T, Ramírez-Portilla C, Sarmiento A, Sánchez JA. Taking a detour: invasion of an octocoral into the Tropical Eastern Pacific. Biological Invasions. 2017; 1–15.
[25] Sánchez JA, Ballesteros D. The invasive snowflake coral (Carijoa riisei) in the Tropical Eastern Pacific, Colombia. Revista de Biología Tropical. 2014;62: 197–207.
[26] Kleypas JA, Langdon C. Coral reefs and changing seawater carbonate chemistry. In: Phinney JT, Hoegh Guldberg O, Kleypas J, Skirving W, Strong A, editors. Coastal and Estuarine Studies. Washington, D. C.: American Geophysical Union; 2006. pp. 73–110.
[27] Feely RA, Sabine CL, Lee K, Berelson W, Kleypas J, Fabry VJ, et al. Impact of anthropogenic CO2 on the CaCO3 system in the oceans. Science. 2004;305: 362–366.
[28] Orr JC, Fabry VJ, Aumont O, Bopp L, Doney SC, Feely RA, et al. Anthropogenic ocean acidification over the twenty-first century and its impact on calcifying organisms. Nature. 2005;437: 681–686.
[29] Caldeira K, Wickett ME. Anthropogenic carbon and ocean pH: Oceanography. Nature. 2003;425: 365–365.
[30] Siegenthaler U, Stocker TF, Monnin E, Luthi D, Schwander J, Stauffer B, et al. Stable Carbon Cycle–Climate Relationship During the Late Pleistocene. Science. 2005;310: 5.
[31] Hoegh-Guldberg O, Poloczanska ES, Skirving W, Dove S. Coral Reef Ecosystems under Climate Change and Ocean Acidification. Frontiers in Marine Science. 2017;4.
[32] Schuhmacher H. Soft corals as reef builders,. In: HA Lessios and IG Macintyre (eds) Proceedings of the 8th International Coral Reef Symposium Vol 1 Smithsonian Tropical Research Institute, Panama. 1997. pp. 99–502.
[33] Jeng M-S, Huang H-D, Dai C-F, Hsiao Y-C, Benayahu Y. Sclerite calcification and reef-building in the fleshy octocoral genus Sinularia (Octocorallia: Alcyonacea). Coral Reefs. 2011;30: 925–933.
[34] Cary LR. The Gorgonaceœ as a Factor in the Formation of Coral Reefs. Carnegie Inst Wash Publ. 1918;213: 341–362.
[35] Millero FJ. The Marine Inorganic Carbon Cycle. Chemical reviews. 2007;107: 308–341.
[36] Manzello DP, Kleypas JA, Budd DA, Eakin CM, Glynn PW, Langdon C. Poorly cemented coral reefs of the eastern tropical Pacific: Possible insights into reef development in a highCO2 world. Proceedings of the National Academy of Sciences. 2008;105: 10450–10455.
[37] Coffroth MA, Lasker HR. Population structure of a clonal gorgonian coral: the interplay between clonal reproduction and disturbance. Evolution. 1998; 379–393.
[38] Sánchez JA, Lasker H. Do multi-branched colonial organisms exceed normal growth after partial mortality? Proceedings of the Royal Society of London. Series B: Biological Sciences. 2004;271 Suppl 3: S117–S120.
[39] Quintanilla E, Madurell T, Wilke T, Sánchez JA. Dynamic Interplay of ENSO Events and Local Hydrodynamic Parameters Drives Demography and Health Status of Gorgonian Sea Fan Populations on a Remote Tropical Eastern Pacific Island. Frontiers in Marine Science. 2019;6.
[40] Inoue S, Kayanne H, Yamamoto S, Kurihara H. Spatial community shift from hard to soft corals in acidified water. Nature Climate Change. 2013;3: 683–687.
[41] Gómez CE, Paul VJ, Ritson-Williams R, Muehllehner N, Langdon C, Sánchez JA. Responses of the tropical gorgonian coral Eunicea fusca to ocean acidification conditions. Coral Reefs. 2015;34: 451–460.
[42] Manzello DP. Coral growth with thermal stress and ocean acidification: lessons from the eastern tropical Pacific. Coral Reefs. 2010;29: 749–758.
*Laboratorio de Biología Molecular Marina (BIOMMAR), Departamento de Ciencias Biológicas, Facultad de Ciencias, Universidad de Los Andes, Bogotá 111711, Colombia.
**Departamento de Biología, Universidad Nacional de Colombia, Bogotá 111321, Colombia.

